風邪をひいて高熱と頭痛に悩むとき、たいていは医者の診察を受ける前に薬局でアスピリン(Aspirin)を買い求め服用する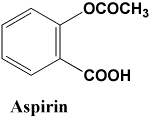 。それでもだめなら医院や病院に駆け込む。おそらく、今日ではこれが大半の人のライフスタイルであろう。アスピリンは医師の処方箋がなくても患者が薬局で直接購入できるいわゆるOTC(over
the counter)の代表であり、解熱鎮痛薬として世界でもっともポピュラーな薬品である。アスピリンは化学的にはアセチルサリチル酸という非常に簡単な有機化合物であり、合成により供給されている。ではアスピリンはどんな経緯で医薬品として確固たる地位を得たのであろうか。
。それでもだめなら医院や病院に駆け込む。おそらく、今日ではこれが大半の人のライフスタイルであろう。アスピリンは医師の処方箋がなくても患者が薬局で直接購入できるいわゆるOTC(over
the counter)の代表であり、解熱鎮痛薬として世界でもっともポピュラーな薬品である。アスピリンは化学的にはアセチルサリチル酸という非常に簡単な有機化合物であり、合成により供給されている。ではアスピリンはどんな経緯で医薬品として確固たる地位を得たのであろうか。
1.アスピリンの起源はヤナギの成分サリシンにある
アスピリンの起源はある種のヤナギの成分であり、歴史的にははるかギリシア時代にまでさかのぼる。当時、もっとも尊敬される医者の 一人にディオスコリデス(Dioscorides, ca.40 - ca.90 AD;右に肖像画を示す)がいたが、その不朽の著作「薬物誌(de Materia Medica)」の中で”セイヨウシロヤナギ(英名white willow)の葉の煎じ薬は通風に著効がある”と述べている。セイヨウシロヤナギは学名をSalix
albaと称するヤナギ科(Salicaceae)植物で、ユーラシア大陸に分布し、欧州の全域で川岸などの水辺に普通に見られる。ディオスコリデス以来、欧州人は何世紀もの間、通風、リウマチ、神経痛、歯痛、耳痛あるいは分娩痛などの痛み止めとしてセイヨウシロヤナギほか数種のヤナギの葉や樹皮の煎じ薬を用いていたのである。その活性成分の単離は多くの科学者が試みたといわれるが、実際に分離されたのは1819年のことでヤナギ(Salix)属の属名に因んでサリシン(Salicin)と命名された。しかし、これは純粋ではなく、実際に結晶化されたのは1827年であり、しかもそれはヤナギからではなく分類学的に関係のないバラ科(Rosaceae)のセイヨウナツユキソウ(Filipendula
ulmaria)の葉に含まれる同一成分であった。
一人にディオスコリデス(Dioscorides, ca.40 - ca.90 AD;右に肖像画を示す)がいたが、その不朽の著作「薬物誌(de Materia Medica)」の中で”セイヨウシロヤナギ(英名white willow)の葉の煎じ薬は通風に著効がある”と述べている。セイヨウシロヤナギは学名をSalix
albaと称するヤナギ科(Salicaceae)植物で、ユーラシア大陸に分布し、欧州の全域で川岸などの水辺に普通に見られる。ディオスコリデス以来、欧州人は何世紀もの間、通風、リウマチ、神経痛、歯痛、耳痛あるいは分娩痛などの痛み止めとしてセイヨウシロヤナギほか数種のヤナギの葉や樹皮の煎じ薬を用いていたのである。その活性成分の単離は多くの科学者が試みたといわれるが、実際に分離されたのは1819年のことでヤナギ(Salix)属の属名に因んでサリシン(Salicin)と命名された。しかし、これは純粋ではなく、実際に結晶化されたのは1827年であり、しかもそれはヤナギからではなく分類学的に関係のないバラ科(Rosaceae)のセイヨウナツユキソウ(Filipendula
ulmaria)の葉に含まれる同一成分であった。

セイヨウシロヤナギ

セイヨウナツユキソウ
サリシンは実際に純薬として使われることはなかった。何故なら、サリシンは内服できないほどひどく苦かったからである(→関連ページ参照、一般に配糖体は苦味の強いものが多い。)。サリシンを含むヤナギの樹皮の煎液も苦く、欧州人は何世紀もの間その鎮痛作用を求めてひたすら苦さに耐えてきたの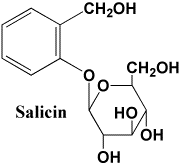 であった。実際にはサリシンやヤナギの樹皮エキスの苦味は日本人の間隔からすればとるに足らないものであった。中国伝統医学では各生薬の味を五味、すなわち辛、酸、甘、苦、鹹に分類している。苦の味を有する薬は五臓の心に作用し心の熱を鎮める作用があるとされ、この作用は苦の味以外の薬で得られない。日本の漢方医学の主流である古方派漢方では五味に触れることはないのだが、中国伝統医学の遺伝子は脈々と受け継がれており、「良薬は口に苦し」という格言まであるように、苦味は薬の本質とされ苦痛とする感性を持ち合わせていないのである。しかし、西洋人はちょっとした苦味も気になるらしく、たとえば苦味のあるものは食べられるものでもまず口にすることはない。サリシンの唯一というべき欠点を克服するため、欧州の科学者たちはその代替品を求め続け、1838年になってサリシンの分解物として得られていたサリチル酸がその任に耐えうることを発見したのである。しかしながら、無味のサリチル酸も内用できる代物ではなかった。刺激作用が激しく、胃の粘膜を確実に損傷するからであった。容易に内用できる鎮痛薬の創製は、19世紀の末、1897年まで待たねばならなかった。ドイツのバイエル社が1899年から販売を開始したアスピリンは以上の過程を経て開発されたアセチルサリチル酸の商品名であり、世界初の合成新薬であった。これ以降、天然成分を化学的に修飾、あるいは全合成により新薬が創製できることが明らかになったわけで、それを可能にする有機合成化学は20世紀以降飛躍的な発展を遂げることになった。アスピリンは比較的安全性の高い薬だが、ピリンの名をもつのでピリン系薬物と誤解されることがある。ピリン系は体質によっては薬物ショックを起こすので一般人からは恐れられているが、アスピリンは完全な非ピリン系薬物である。アスピリンの名はその直接の原料となったサリチル酸のドイツ名スピールゾイレ(spir
saure)に因む。更に、スピールゾイレはセイヨウナツユキソウのラテン異名であるSpiraea
ulmariaの属名スピレア(Spiraea)に由来しているが、初めて純粋物質として得られたのがヤナギではなくセイヨウナツユキソウであったからである。また、アスピリンはバイエル社の登録商品名であったが、第一次大戦後、敵対国であるという理由で各国で登録が抹消され、一般名となった。わが国でも1932年以来日本薬局方にアスピリンの一般名で収載されている。
であった。実際にはサリシンやヤナギの樹皮エキスの苦味は日本人の間隔からすればとるに足らないものであった。中国伝統医学では各生薬の味を五味、すなわち辛、酸、甘、苦、鹹に分類している。苦の味を有する薬は五臓の心に作用し心の熱を鎮める作用があるとされ、この作用は苦の味以外の薬で得られない。日本の漢方医学の主流である古方派漢方では五味に触れることはないのだが、中国伝統医学の遺伝子は脈々と受け継がれており、「良薬は口に苦し」という格言まであるように、苦味は薬の本質とされ苦痛とする感性を持ち合わせていないのである。しかし、西洋人はちょっとした苦味も気になるらしく、たとえば苦味のあるものは食べられるものでもまず口にすることはない。サリシンの唯一というべき欠点を克服するため、欧州の科学者たちはその代替品を求め続け、1838年になってサリシンの分解物として得られていたサリチル酸がその任に耐えうることを発見したのである。しかしながら、無味のサリチル酸も内用できる代物ではなかった。刺激作用が激しく、胃の粘膜を確実に損傷するからであった。容易に内用できる鎮痛薬の創製は、19世紀の末、1897年まで待たねばならなかった。ドイツのバイエル社が1899年から販売を開始したアスピリンは以上の過程を経て開発されたアセチルサリチル酸の商品名であり、世界初の合成新薬であった。これ以降、天然成分を化学的に修飾、あるいは全合成により新薬が創製できることが明らかになったわけで、それを可能にする有機合成化学は20世紀以降飛躍的な発展を遂げることになった。アスピリンは比較的安全性の高い薬だが、ピリンの名をもつのでピリン系薬物と誤解されることがある。ピリン系は体質によっては薬物ショックを起こすので一般人からは恐れられているが、アスピリンは完全な非ピリン系薬物である。アスピリンの名はその直接の原料となったサリチル酸のドイツ名スピールゾイレ(spir
saure)に因む。更に、スピールゾイレはセイヨウナツユキソウのラテン異名であるSpiraea
ulmariaの属名スピレア(Spiraea)に由来しているが、初めて純粋物質として得られたのがヤナギではなくセイヨウナツユキソウであったからである。また、アスピリンはバイエル社の登録商品名であったが、第一次大戦後、敵対国であるという理由で各国で登録が抹消され、一般名となった。わが国でも1932年以来日本薬局方にアスピリンの一般名で収載されている。
2.アスピリンの主要薬効は血栓予防である
アスピリンは発売以来100年以上になるが、今日でも世界で年間100億錠以上消費される。米国ではアスピリンは薬局ではなく、スーパーやコンビニエンスストアで食品や日用雑貨品とともに販売されているほどで、もっとも気軽に入手できる薬である(わが国でも検討されている)。アスピリンの本来の適用薬効は解熱鎮痛であるが、そのメカニズムが解明されたのは意外に新しい。1971年、アスピリンがプロスタグランジン(Prostaglandin; PG)の鍵生合成酵素であるシクロオキシナーゼ(cyclooxygenase)を阻害することが発見された(図参照)。体内での発熱は感染、組織破壊、炎症などの病的状態の結果として起きるのであるが、この時プロスタグランジンの一種であるPGE2の生合成が視床下部内で促進され、PGE2がcyclicAMPに媒介される過程を活性化して体温が上昇する。アスピリンはPGE2の生合成を阻害することで解熱作用を示すのであるが、正常値より体温が下がることはなく、また運動や環境温度の上昇などによって上昇した体温に対して影響を与えない。アスピリンは頭痛、筋肉痛、関節痛などの鎮痛に効果があるが、これもプロスタグランジンの生合成阻害によるものである。プロスタグランジンは機械的あるいは化学的刺激に対する疼痛受容体を感作させる働きがあるからである。アスピリンの鎮痛効果はモルヒネの10分の1にすぎないが、長期投与しても耐性、嗜癖はなく毒性も低いので広く用いられたが、今日ではアセトアミノフェンに代替されている。とりわけ、慢性の術後痛や炎症による痛みではアスピリン(→アセトアミノフェン)によりもっともよい疼痛コントロールが得られる。欧米では、アスピリン(→アセトアミノフェン)は鎮痛目的、それもリウマチなどの関節痛で多用され、わが国とは違って解熱薬という意識は希薄である。前述したように、アスピリンは既に古典的薬物といってよいものであるが、現在、消費量はむしろ増加の傾向にある。2001年から、アスピリンの適用薬効として解熱、鎮痛のほか、心筋梗塞および脳梗塞再発予防作用が加えられた。アスピリンには血栓を予防する効果のあることは1950年代から指摘されており脳梗塞や狭心症の予防に効果があるといわれてきた。1988年、このようなアスピリンの効能を裏付ける注目すべき論文が米国の権威ある医学雑誌"New England Journal of Medicine"に掲載された。これは40歳以上の健康な医師22,071人をA、B二つのグループに分け、Aグループでは325mgのアスピリンを隔日投与、Bグループではプラシーボ(偽薬)としてデンプン錠を同様に投与し、二重盲検法により5年間の長期にわたって追跡調査を行った。その結果、Aグループでは104人の心臓発作患者が発生し、5人が死亡したのに対し、Bグループでは189人の発作患者中18人が死亡した。つまり、アスピリン投与群では発生率、死亡率ともにプラシーボ群に比べて有意の差をもって低い結果を得たのである。他の注目すべき知見として、アスピリン投与群では皮下出血や鼻出血などの頻度が32%大きく、輸血が必要とされたものの頻度も71%高いという結果が得られた。これはアスピリン投与による抗血小板作用の結果と考えられる。本論文の他にもアスピリンが狭心症や心筋梗塞の予防に効果があるという報告があるが、New England Journal of Medicine誌の論文がもっとも信頼できるデータを提供したとされ、以降米国では当該目的でアスピリンが本格的に使用されることになったのである。アスピリンは血小板の作用を抑制して血栓の生成を抑制するのであるが、これはアスピリンの少量投与でもっとも効率よく抑制され、大量投与ではむしろその効果は減弱する。これはいわゆる”アスピリンジレンマ”と呼ばれるものであり、次のように説明される。すなわち、血小板に対して相反する作用をもつトロンボキサンA2とPGI2の2つの因子があり、前者は血小板の機能を亢進して血小板を凝集させたり血管を収縮させたりする作用があり、後者は血小板の機能を抑制して血小板の凝集を抑えたり血管を拡張させたりする作用がある。トロンボキサンA2、PGI2ともにアラキドン酸からシクロオキシナーゼにより生合成されるものである(図参照)が、トロンボキサンA2をつくるシクロオキシゲナーゼは血小板内にあるのに対し、PGI2をつくるシクロオキシゲナーゼは血管内皮細胞に存在する。アスピリンは血管内皮細胞のシクロオキシゲナーゼ よりも血小板のシクロオキシゲナーゼ に対し高い親和性をもつので、低用量でもトロンボキサンA2の生合成を抑制できるが、高用量では血管内皮細胞のシクロオキシゲナーゼも阻害してPGI2の生合成を阻害してしまうので、全体として血栓抑制のの効果が減弱してしまうのである。以上、アスピリンの抗血栓作用は揺るぎない事実といってよいが、New England Journal of Medicine誌の論文でも指摘されているように、止血という観点でとりわけ注意を要する。例えば、外科手術や歯科での抜歯を受ける場合は、直ちにアスピリンの服用をとめる必要がある。アスピリンによるシクロオキシゲナーゼの阻害作用は非可逆的であるので服用をとめてもすぐにアスピリンの作用から抜け出ることはできず、新たに生成する血小板で置き換えられるまで待たねばならない。一般に、その期間は9日とされているので、出血を伴う手術を受ける場合、アスピリンの服用停止から9日以上待たねばならないことになる。解熱鎮痛薬としてアスピリンを服用する場合、一日最大で2~3gであり、その錠剤も250~330mgと用量が大きい。しかし、抗血栓薬としては1日80~160mgが適当とされるので、解熱鎮痛薬用の錠剤は服用できない。以前は医療用「小児用バファリン(81mg錠)」が転用されていたが、薬局で入手できるOTCの「小児用バファリン」はアスピリンではなく抗血栓作用のないアセトアミノフェンでこれに伴うトラブルが頻発した。現在では、アスピリンの薬効適用が拡大されたのに伴い抗血小板薬「バファリン81mg錠」が2001年より発売され、また医療用「小児用バファリン(81mg錠)」の販売は中止されトラブルは解消している。
3.アスピリンの副作用について
アスピリンは比較的副作用の少ない薬であるが、皆無ではない。主要な副作用として胃組織の損傷がある。これはアスピリンが胃酸の粘膜内への逆拡散を促し、またプロスタグランジンによる胃酸分泌抑制の効果が生合成阻害により失われるためである。しかし、この副作用は腸溶錠の使用により大幅に軽減することができる。わが国ではアスピリンはダイアルミネート製剤(緩衝錠)が主流であり、腸内で溶けるよう設計されている腸溶錠に比べて胃障害が必然的に多かった。米国では98%はアスピリン腸溶錠であるとの報告があるが、わが国では米国よりかなり遅れて腸溶錠が普及したが、腸溶錠は緩衝錠に比べてコストが格段に高くなる。アスピリンが副作用として胃障害を起こすことは一般に広く定着しており、これを説得して腸溶錠を勧めるのは薬剤師の職務の重要な部分であろう。アスピリンはシクロオキシゲナーゼを阻害するのでロイコトリエンが増加する。その結果として気管支喘息を誘発することがあり、これをアスピリン喘息と呼ぶことがある。また、突発性の激しい発作を誘発することがあるので、特に喘息患者へのアスピリンの投与は控えるべきである。その他、因果関係が証明されたわけではないが、米国においてインフルエンザや水痘などのウイルス性疾患に解熱剤としてアスピリンを用いた小児にライ症候群が多発したため、医薬品等安全性情報として厚生労働省から幼児にアスピリンの使用を控えるよう注意喚起がなされている。小児用バファリンがアスピリンではなくアセトアミノフェンであるのもそのためである。
↑ページトップへ戻る